Радиационно-химический выход - число молекул вещества, образовавшегося или разложившегося в системе, подвергающейся действию ионизирующего излучения, при поглощении системой энергии в 100 эВ.
Радикалы свободные - атомы или химические соединения с неспаренным электроном (обозначается жирной точкой), напр.
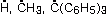 . Парамагнитны, реакционноспособны. Короткоживущие радикалы — промежуточные частицы во многих химических реакциях. Некоторые радикалы свободные стабильны и выделены в индивидуальном состоянии. С участием радикалов свободных осуществляются важные биохимические процессы, напр. ферментативное окисление.
. Парамагнитны, реакционноспособны. Короткоживущие радикалы — промежуточные частицы во многих химических реакциях. Некоторые радикалы свободные стабильны и выделены в индивидуальном состоянии. С участием радикалов свободных осуществляются важные биохимические процессы, напр. ферментативное окисление.
Радиолиз (от радио... и ...лиз) - химическое или физико-химическое превращение вещества под действием ионизирующих излучений. Радиолиз — предмет изучения радиационной химии; актуальные проблемы — радиолиз газов при высоких температурах, радиолиз воды и водных растворов при сверхкритических температурах, влияние дефектов и примесей на радиолиз твердых тел.
Радиопротекторы (от радио... и лат. protector — защитник) - химические соединения, повышающие устойчивость организма к действию ионизирующих излучений (путем создания аноксии, нейтрализации ионизированных атомов и молекул и др.). Вводят в организм перед облучением, напр. при лучевой терапии злокачественных опухолей. К эффективным радиопротекторам относятся вещества, содержащие сульфгидрильные группы, некоторые амины, полимеры и др.
Рассеянные элементы - группа химических элементов, как правило, не образующих самостоятельных минералов (присутствуют в виде изоморфных примесей в минералах более распространенных элементов). Типичные рассеянные элементы — рубидий, галлий, гафний, германий и др.
Растворимости диаграмма - см. Диаграмма состояния.
Растворимость - способность вещества в смеси с одним или несколькими другими веществами образовывать растворы. Мера растворимости вещества в данном растворителе — концентрация его насыщенного раствора при данных температуре и давлении. Растворимость газов зависит от температуры и давления, растворимость жидких и твердых тел практически от давления не зависит.
Растворители - неорганические (главным образом вода) или органические (бензол, хлороформ, ацетон, спирты и др.) вещества, а также смеси (напр., бензин), способные растворять различные вещества. Основные требования: минимальные токсичность и пожароопасность, химическая инертность по отношению к растворяемому веществу, доступность и дешевизна; важные свойства растворителей — плотность, вязкость, диэлектрическая проницаемость, показатель преломления.
Растворы - однородные смеси переменного состава двух или большего числа веществ (компонентов). Могут быть газовыми (напр., воздух), жидкими и твердыми (напр., многие сплавы). В жидких растворах компонент, находящийся в избытке, называется растворителем, все остальные компоненты — растворенные вещества. По концентрации растворенного вещества растворы подразделяют на насыщенные, ненасыщенные и перенасыщенные. В растворах протекают многие природные и промышленные процессы; изучение свойств растворов связано с такими практическими проблемами, как разделение веществ (газов, нефтей), глубокая очистка, подбор растворителей для реализации технологических процессов.
Рауля закон - относительное понижение давления насыщенного пара растворителя над разбавленным раствором равно молярной доле растворенного вещества
N:( po — p1)/ po = N, где po и
p1 — соответствующее давление насыщенного пара чистого растворителя и растворителя над раствором.
Рацематы (рацемические соединения)
- см. в ст. Энантиомерия.
Реакции химические -
превращения одних веществ в другие,
отличные по химическому составу и (или)
строению. Характеризуются
стехиометрическим соотношением
участвующих в них веществ, степенью
превращения, константами скорости и
равновесия, энергией активации, тепловым
эффектом. Химические реакции
классифицируют по числу молекул,
участвующих в элементарном акте (моно-,
бимолекулярные), кинетическому механизму (последовательные,
параллельные, сопряженные), характеру
химического процесса (разложение,
окисление, полимеризация и др.), типам
частиц, участвующих в химических реакциях (ионные,
радикальные), фазовому состоянию
реагирующей системы (газо-, жидко- и
твердофазные). Гомогенные химические
реакции протекают в объеме фазы,
гетерогенные — на поверхности раздела фаз.
Редкие металлы - название
группы металлов (св. 50), использующихся в
небольших количествах или относительно
новых в технике. Количество редких металлов
в земной коре составляет 0,53% по массе (0,41%
приходится на титан). К редким металлам
относят: элементы I группы периодической
системы — Li, Rb, Cs, Fr; II группы — Be, Ra; III группы
— Ga, In, Tl, Sc, Y, La, Ac, лантаноиды и актиноиды; IV
группы — Ti, Zr, Hf; V группы — V, Nb, Ta; VI группы —
Mo, W, Po; VII группы — Re, Tc. По мере увеличения
производства этих элементов термин «редкие
металлы» становится все более условным.
Резонанса теория - в химии —
концепция, дополняющая постулаты
классической теории химического строения и
утверждающая, что если для данного
соединения классическая теория допускает
построение нескольких приемлемых
структурных формул, то действительному
состоянию молекул этого соединения (его
химическим свойствам) отвечает не какая-либо
одна отдельная формула, а некоторое их
сочетание (наложение, резонанс структур).
Резонанса теория предложена Л. Полингом в
1928-31.
Ржавчина - слой частично
гидратированных оксидов железа,
образующийся на поверхности железа и
некоторых его сплавов в результате
коррозии, вызванной действием кислорода и
влаги.
Ряд напряжений (ряд активностей)
в электрохимии - последовательность
расположения металлов в порядке
возрастания значений из стандартного
потенциала (за нуль принят потенциал
водорода). Ряд напряжений некоторых
металлов: К, Са, Mg, Al, Zn, Cr(III), Fe(II), H2, Cu, Ag,
Hg, Au. Каждый металл вытесняет из растворов
солей металлы, стоящие справа от него;
металлы, которые расположены левее Н2,
вытесняют его из кислот.

